Este artículo fue publicado y traducido bajo los términos de nuestra licencia con Jobson Healthcare Information. Queda estrictamente prohibida su reproducción total o parcial.
Por John D. Gelles, OD1,2,3
1. Director de la División de Lentes de Contacto Especializadas del Instituto de Córnea y Láser Ocular (CLEI) y del Centro CLEI para el Queratocono, en Teaneck, Nueva Jersey.
2. Se desempeña como profesor clínico asistente en el Departamento de Oftalmología y Ciencias Visuales de la Facultad de Medicina de Rutgers–New Jersey, y como profesor clínico adjunto en la Facultad de Optometría de Illinois, la Facultad de Optometría de Nueva Inglaterra y la Facultad de Optometría de la Universidad Estatal de Nueva York.
3. En este artículo se revisará cómo comunicar de manera eficaz un enfoque integral en tres frentes y definir con claridad los pasos a seguir en el manejo del queratocono, lo que puede ayudar a reducir la ansiedad del paciente y mejorar su adherencia al tratamiento.
A lo largo de los años, se han publicado numerosos artículos sobre el diagnóstico del queratocono (KC); sin embargo, son pocos los que abordan cómo comunicarse de manera eficaz con los pacientes que reciben este diagnóstico por primera vez. Nuestra clínica, The Cornea & Laser Eye Institute, ubicada en Teaneck, Nueva Jersey, es una institución especializada en córnea y cirugía refractiva, fundada en 1995, que cuenta con un centro subespecializado: el CLEI Center for Keratoconus.
Desde su creación, en el año 2001, este centro se ha dedicado de forma continua a la investigación, el desarrollo de tratamientos y el manejo integral del queratocono. Actualmente, esta patología representa la mayor parte de nuestras consultas clínicas anuales y actividades de investigación. Gracias a esta amplia experiencia en el manejo cotidiano del queratocono, hemos podido optimizar la manera en que abordamos a los pacientes tras el diagnóstico e identificar qué tipo de lenguaje logra una mejor conexión con ellos.
Aunque el diagnóstico del queratocono ha sido ampliamente abordado en la literatura científica, existe un número limitado de publicaciones centradas en cómo comunicar esta condición eficazmente a los pacientes recién diagnosticados. A partir de la experiencia clínica y de investigación desarrollada por el The Cornea & Laser Eye Institute, fundado en 1995 en Nueva Jersey y, por su centro subespecializado, el CLEI Center for Keratoconus, dedicado desde 2001 al estudio y manejo integral de esta enfermedad, los autores han optimizado el abordaje comunicativo con estos pacientes. Esta experiencia ha permitido identificar estrategias y un lenguaje clínico que favorecen la comprensión del diagnóstico, disminuyen la ansiedad y fortalecen la relación profesional entre el profesional de la salud visual y el paciente.
A medida que los tratamientos para el queratocono han evolucionado, también lo ha hecho nuestra forma de comunicarnos. En octubre de 2025 y, con las opciones terapéuticas actualmente disponibles, hemos logrado implementar un modelo educativo integral y centrado en el paciente, que ha demostrado ser eficaz para mejorar su comprensión de la enfermedad y favorecer resultados clínicos exitosos a largo plazo.
La conversación
Recibir un diagnóstico de queratocono puede resultar abrumador para el paciente; sin embargo, este momento representa una oportunidad clave para establecer expectativas claras y una estrategia específica y estructurada para su atención. Iniciamos la conversación con una explicación accesible y fácil de comprender sobre la enfermedad. Para ello, utilizamos la analogía de la córnea como el lente frontal de una cámara, destacando que su curvatura precisa es fundamental para lograr una visión nítida.
En el queratocono, esta curvatura se altera, lo que genera pérdida de claridad visual y distorsión de la imagen. Este proceso ocurre como consecuencia de una debilidad focal y adelgazamiento progresivo de la córnea; de manera similar a un punto delgado y frágil en una pelota o un neumático que se abomba hacia afuera, la córnea queratocónica presenta una protrusión localizada que compromete su función óptica.
Aquí nos detenemos para revisar conjuntamente las mediciones de tomografía y aberrometría, acompañadas de explicaciones sencillas, cómo aclarar que los colores más cálidos indican áreas de mayor elevación, irregularidad, adelgazamiento o distorsión. La revisión de simulaciones visuales basadas en la aberrometría puede ayudar a conectar con los pacientes, al demostrar comprensión de su experiencia y validar sus quejas visuales.
Revisión de los factores de riesgo
Todos los pacientes recién diagnosticados quieren saber tres cosas: si se quedarán ciegos, si la KC es genética y si pueden hacer algo para ayudar a detenerla. Para responder a la primera: la KC es una enfermedad progresiva que, si no se trata, puede conducir a una reducción profunda de la visión y de la calidad de vida; sin embargo, con una atención adecuada, su progresión puede detenerse y la calidad de vida relacionada con la visión del paciente puede mejorar mediante el uso de lentes de contacto u opciones quirúrgicas. Nuestra siguiente conversación girará en torno a la genética y a los principales factores de riesgo asociados con la KC: antecedentes familiares, frotamiento ocular y enfermedades asociadas. ²⁹
La genética del queratocono es compleja, ya que no existe un «gen del KC». Más bien, hasta ahora se conocen alrededor de 36 regiones de nuestro ADN que se asocian con la enfermedad.³⁰ Se recomienda encarecidamente realizar pruebas de detección de queratocono a los familiares para permitir un diagnóstico y una intervención más tempranos, especialmente en la población pediátrica.³¹ En el caso de los familiares con síndrome de Down, el cribado es particularmente importante debido a la mayor prevalencia de la enfermedad en esta población.³²,³³ Eduque al paciente sobre la importancia de evitar el frotamiento ocular, ya que este estrés mecánico puede acelerar el debilitamiento biomecánico de la córnea y constituye un factor de riesgo modificable relacionado con el comportamiento.³⁴,³⁵ Aborde y maneje de forma proactiva, o derive para su tratamiento, las afecciones asociadas como alergias, atopia, asma y apnea.
Revisión de las opciones de tratamiento
Hemos comprobado que la forma más sencilla de educar a los pacientes es introducirles el concepto de «Queratocono 1, 2, 3». Este enfoque para el manejo del KC es fácil de recordar: uno, estabilizar; dos, contornear; y tres, mejorar la visión. Lo más importante es presentar de manera general los tres conceptos, ya que esto contribuye a que el paciente esté bien informado, sea consciente de que existen múltiples opciones de tratamiento y se sienta motivado. No todos los pacientes necesitarán todas las opciones, no es obligatorio seguir un orden específico y no todas deben aplicarse de forma independiente.
Los días en los que solo existían dos opciones —lentes rígidas permeables al gas (RGP) y queratoplastia penetrante— han quedado atrás. Hoy, el enfoque se centra en un manejo intervencionista del KC: diagnosticar e intervenir de forma temprana para preservar y restaurar la visión. A continuación, se describen con mayor detalle las tres categorías.
1. Estabilizar.
El entrecruzamiento corneal es un procedimiento destinado para estabilizar la córnea y representa el avance más importante en el manejo del KC; es fundamental y constituye la piedra angular del tratamiento moderno. A continuación, describimos la importancia del CXL. El CXL actúa aumentando los enlaces intermoleculares, fortaleciendo el tejido corneal debilitado por el queratocono y, de este modo, deteniendo su progresión. El CXL por sí solo no mejora la visión ni está diseñado para hacerlo; su objetivo es prevenir un mayor deterioro. Para los pacientes, solemos explicarlo como algo similar a añadir cables a un puente o barras de refuerzo a un edificio.
| Preparación de los pacientes para la CXLDescribimos el procedimiento de entrecruzamiento corneal como largo, pero no estresante. A los pacientes les explicamos que adormeceremos el ojo para su comodidad y que, posteriormente, colocaremos un separador palpebral para evitar el parpadeo durante el procedimiento. A continuación, retiraremos las células de la superficie de la córnea y, durante 30 minutos, aplicaremos gotas de riboflavina sobre la córnea. Después, el paciente mirará una luz ultravioleta durante otros 30 minutos. Al finalizar el procedimiento, utilizaremos una lente de contacto tipo vendaje para cubrir la córnea, lo que ayudará a reducir el dolor y a favorecer la regeneración de la capa celular. Tras el procedimiento, el paciente deberá aplicarse dos gotas, cuatro veces al día: un antibiótico para prevenir infecciones y un esteroide para reducir la inflamación. La mayoría de los pacientes presentará dolor ocular, lagrimeo y sensibilidad a la luz una vez que lleguen a casa y durante las primeras 24 a 72 horas después de la CXL. La intensidad del dolor varía de una persona a otra, pero generalmente se describe como dolor sordo y pulsátil. La primera tarde suele ser la parte más difícil de la recuperación. Con cada día que pasa, el dolor irá disminuyendo y, por lo general, al tercer día lo peor del dolor habrá pasado; sin embargo, es posible que persista la sensación de sequedad o de cuerpo extraño. Dormir lo suficiente, aplicar compresas frías y utilizar analgésicos de venta libre ayudará a aliviar los síntomas. A continuación, les explicamos que los veremos al día siguiente del procedimiento para asegurarnos de que todo haya salido bien. Entre cinco y siete días después de la CXL, los volveremos a ver y retiraremos la lente de contacto tipo vendaje, una vez que la capa celular haya vuelto a crecer y la córnea esté cicatrizando según lo previsto. En ese momento, suspenderán el uso de las gotas antibióticas, comenzarán a utilizar lágrimas artificiales sin conservantes para mantener el ojo húmedo y ayudar a que la capa celular se alise, y reducirán gradualmente las gotas de esteroides en una gota por semana hasta suspenderlas por completo al cumplir un mes. Una vez más, los veremos al cumplir un mes para supervisar su evolución. La mayoría de los pacientes experimenta cambios visuales leves y temporales, así como opacidad corneal, los cuales suelen mejorar entre la visita de los tres y seis meses. Pueden reanudar el uso de lentes de contacto entre dos y cuatro semanas después del CXL, dependiendo del tipo de lente utilizado y de cómo haya sido el proceso de cicatrización. Tres meses después del procedimiento y cada seis meses a partir de entonces, supervisaremos la córnea para detectar cualquier cambio. Es fundamental continuar con el seguimiento según las indicaciones.El CXL es un procedimiento muy seguro y eficaz; sin embargo, como ocurre con cualquier intervención, conlleva ciertos riesgos. Entre ellos se incluyen el retraso en la cicatrización, la infección y la formación de cicatrices, lo que puede dar lugar a una reducción de la visión. Afortunadamente, estas complicaciones son poco frecuentes. Se ha demostrado que el CXL proporciona estabilidad a largo plazo; no obstante, algunos pacientes pueden continuar presentando progresión incluso después del CXL y podrían requerir un nuevo tratamiento. |
2. Contorno
Existen diversas técnicas para optimizar la forma de la córnea y mejorar el potencial visual cuando no se utilizan lentes de contacto. Las dos cirugías corneales mínimamente invasivas más modernas para este propósito son la queratectomía fotorrefractiva guiada por topografía (TGPRK) y la queratoplastia con adición de tejido corneal (CTAK). A los pacientes les explicamos que estamos remodelando la córnea ya sea mediante la eliminación o la adición de tejido corneal en ubicaciones específicas, con el objetivo de hacerla más simétrica.
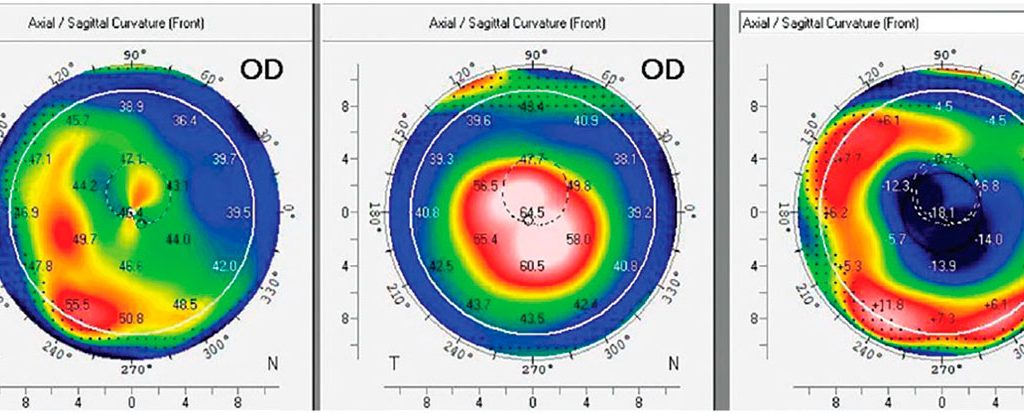
Este paciente se sometió a una cirugía CTAK. Presentaba complicaciones derivadas del uso excesivo de lentes esclerales debido a una visión no funcional sin lentes. La cirugía CTAK proporcionó un aplanamiento de 18,9 D en el punto máximo y una forma corneal central mucho más regular. La visión mejoró de 20/400 sin corrección, 20/200 con refracción manifiesta y 20/50 con uso de lentes esclerales a 20/40 sin corrección, 20/25 con refracción manifiesta y 20/25 con uso de lentes de contacto blandas. Las complicaciones derivadas del uso excesivo se resolvieron, ya que el paciente pudo funcionar sin lentes de contacto, lo que permitió reducir el tiempo de uso. Mapa de izquierda a derecha: postoperatorio; preoperatorio; mapa de diferencias que muestra los cambios en la forma de la córnea.
Los pacientes que suelen beneficiarse más de la CTAK y la TGPRK presentan limitaciones visuales significativas con el uso de gafas; en general, deben tener una agudeza visual mejor corregida con gafas inferior a 20/25. Es importante pedir a los pacientes que reflexionen sobre su calidad de vida al usar gafas y si una mejoría en la visión con corrección óptica tendría un impacto significativo en ella. Este diálogo centrado en el paciente ayuda a determinar su interés en los procedimientos de contorneado corneal.
En pacientes con catarata o en aquellos que podrían considerar opciones como lentes de colámero implantables (ICL) o intercambio refractivo del cristalino, la realización de CTAK o TGPRK permite obtener una córnea más regular, lo que facilita mediciones y cálculos más precisos, mejorando así la exactitud en la potencia del implante y el resultado visual final.
No realizamos TGPRK en pacientes menores de 18 años; sin embargo, pueden considerarse otros procedimientos de modificación de la curvatura corneal. Los trasplantes de córnea deben reservarse para restaurar la claridad y la curvatura corneal. En pacientes con cicatrices corneales significativas y enfermedad avanzada, la sobre-refracción con lentes de contacto es útil para determinar si es razonable considerar un trasplante. Si la visión mejora, el principal problema es la forma de la córnea; si no hay mejoría, la cicatriz es visual y funcionalmente significativa, y el trasplante puede estar indicado cuando la visión alcanzada no es adecuada para las actividades de la vida diaria.
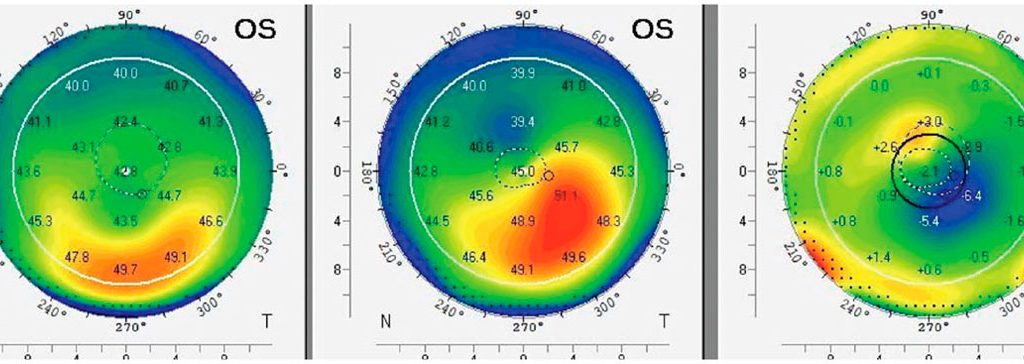
Este paciente se sometió a CXL en el ojo izquierdo (OI) y se perdió el seguimiento antes de recibir tratamiento en el ojo derecho (OD). A lo largo de 12 meses, el ojo derecho progresó 2.40 D, mientras que el ojo izquierdo presentó un aplanamiento de 2.60 D. Este caso pone de manifiesto la importancia de la educación del paciente y del seguimiento a largo plazo.
De izquierda a derecha, los mapas muestran: posoperatorio, preoperatorio y mapa de diferencias, que ilustra los cambios en la forma corneal.
Por último, la visión es el aspecto que más preocupa a los pacientes y esperan que se les proporcione de manera oportuna. El momento adecuado del tratamiento suele generar inquietud, con preguntas frecuentes como: “¿CXL o lentes de contacto?, ¿cuál debe realizarse primero?”. En la práctica, debe iniciarse aquello que pueda comenzar de inmediato, evitando retrasar el tratamiento.
Cada uno de los procedimientos aquí mencionados se realiza de forma unilateral, lo que permite que el ojo contralateral pueda someterse simultáneamente a la adaptación de lentes de contacto. En la mayoría de los casos, el CXL no produce cambios clínicamente significativos en la curvatura corneal que obliguen a una readaptación completa, independientemente del tipo de lente utilizado. En contraste, la CTAK o la TGPRK sí generan cambios sustanciales en la curvatura corneal y pueden requerir una readaptación de las lentes que se apoyan sobre la superficie corneal. Es poco probable que una lente escleral bien adaptada antes de cualquiera de estos procedimientos necesite modificaciones en la profundidad sagital o en los parámetros de la zona de aterrizaje; no obstante, en algunos casos —aunque no en todos— puede ser necesario un ajuste de la potencia.
Tras un procedimiento, la corrección visual con lentes de contacto suele poder reanudarse o iniciarse a las cuatro semanas, independientemente de que se trate de lentes rígidas o blandas. Las lentes blandas estándar y las esclerales pueden utilizarse incluso antes si la situación clínica lo requiere. Como regla general, no debe retrasarse un tipo de atención en favor de otro; lo fundamental es que el paciente comprenda la necesidad de cada intervención, sea acompañado a lo largo del proceso y no quede sin seguimiento.
Los pacientes que reciben lentes de contacto antes del CXL con frecuencia olvidan la importancia de este último para detener la progresión de la enfermedad. Es esencial recordarles que el hecho de ver mejor no implica que el proceso patológico se haya detenido, sino que se requiere un seguimiento continuo y tratamiento con CXL cuando esté indicado, con el fin de lograr una visión adecuada y preservar su calidad de vida.
El plan para el paciente
A partir de este punto, la educación general debe dar paso a la presentación de un plan individualizado para cada paciente. Es clave retomar el enfoque de Queratocono 1, 2, 3, pero adaptándolo a la situación específica del paciente y destacando con claridad los pasos inmediatos más importantes.
Los pacientes recién diagnosticados menores de 20 años deben ser derivados de forma inmediata para CXL y, al mismo tiempo, programar una cita para iniciar el proceso de adaptación de lentes de contacto médicas. En cambio, en los pacientes recién diagnosticados mayores de 20 años, el siguiente paso debe ser comenzar la adaptación de lentes de contacto médicas y agendar una cita de control a los tres meses para regresar a la clínica y vigilar la progresión. Si existe interés en mejorar la visión con gafas, puede considerarse una derivación para contorneado corneal.
Independientemente del perfil del paciente, es imprescindible enfatizar la necesidad de un seguimiento estrecho, reiterando que el queratocono es una enfermedad progresiva e impredecible, pero que seguir un plan estructurado puede limitar su impacto e incluso mejorar la calidad de vida del paciente.
Conclusiones
El manejo del queratocono es un trabajo en equipo. Contar con un plan bien establecido entre el médico tratante, el cirujano y el paciente es fundamental para lograr resultados exitosos, y el grado de participación de cada uno dependerá del nivel de experiencia y de los recursos disponibles para la atención. Es recomendable incorporar las herramientas diagnósticas necesarias, como la tomografía corneal, y mantenerse actualizado sobre los avances en el manejo si el tratamiento de estos pacientes forma parte de su interés clínico.
Asimismo, es importante establecer vínculos y realizar derivaciones a cirujanos con experiencia en la amplia gama de opciones terapéuticas disponibles para esta población, así como colaborar con colegas que cuenten con experiencia en lentes de contacto médicos. Como médico remitente, es preferible mantener una derivación amplia, evitando definir de antemano el procedimiento específico o el tipo exacto de lente de contacto, ya que los planes contradictorios pueden generar confusión y pérdida de confianza en el paciente.
En última instancia, el manejo del queratocono desde el primer día requiere una comunicación clara y la programación de un siguiente paso concreto, ya sea mediante referencia o comanejo. La implementación total, parcial o nula de las estrategias descritas en este artículo queda a criterio del lector; sin embargo, nuestro objetivo es invitar a la reflexión sobre los métodos actuales y mejorar la comunicación con los pacientes recién diagnosticados, ya que esto se traduce en pacientes mejor informados y resultados clínicos más exitosos.
Referencia:
Review of Optometry. (s. f.). My patient has keratoconus—now what? Review of Optometry. https://www.reviewofoptometry.com/article/my-patient-has-keratoconus-now-what